- Nghiên cứu ALBIOS: ngày 0 và ngày 1 được truyền 400 mL albumin 20%, sau đó truyền albumin 20% để duy trì albumin máu >30 g/L.
- Nghiên cứu EARSS: albumin 20% 100 mL mỗi 8 giờ trong 3 ngày đầu.
- Nghiên cứu SAFE: hồi sức bằng albumin 4% (bất kỳ khi nào cần bù dịch thay cho dịch tinh thể).
- Nghiên cứu CRISTAL: albumin 4-5% trong nhóm dịch keo với áp suất keo thấp, albumin 20-25% trong nhóm dịch keo với áp suất keo cao.
----
Hồi sức dịch là thực hành tiêu chuẩn cho các tình trạng huyết động không ổn định tương đối hoặc tuyệt đối nhằm phục hồi và duy trì tưới máu mô. Nguy cơ đáng kể của liệu pháp dịch có liên quan đến việc truyền chưa đủ hoặc quá nhiều, cũng như các tác dụng phụ dược lý của loại dịch được sử dụng. Hàng ngày, có hơn 20% bệnh nhân tại các khoa hồi sức tích cực (ICU) được điều trị bằng dịch truyền tĩnh mạch; hơn 30% được truyền dịch để hồi sức thể tích vào ngày thứ nhất nhập ICU.
Ngoại trừ sốc tim, các loại sốc còn lại đều cần hồi sức dịch hoặc cần truyền dịch để làm tăng thể tích tuần hoàn. Những tranh luận về ưu và nhược điểm của từng loại dịch truyền so với loại kia vẫn còn kéo dài và dữ liệu hiện tại chưa thể khẳng định dứt khoát rằng loại dịch nào là tốt nhất. Tùy thuộc vào từng bối cảnh, từng trường hợp và từng thời điểm hồi sức dịch, dịch tinh thể hoặc dịch keo mang lại các lợi ích và tác hại khác nhau. Nếu như dịch tinh thể đã được đồng thuận là loại dịch truyền đầu tay trong hồi sức sốc thì các loại dịch keo, đặc biệt là dung dịch albumin huyết thanh người (human serum albumin - HSA), vẫn có thể có những vai trò nhất định do được giữ lâu trong lòng mạch, có hiệu quả thể tích tốt và ít tác dụng phụ nhưng khá đắt tiền. Việc sử dụng dịch albumin sao cho hiệu quả đòi hỏi hiểu biết tốt về đặc tính sinh lý, chức năng của phân tử albumin, nguyên tắc hồi sức dịch và hiệu quả lâm sàng của dung dịch albumin.
Cả cấu trúc phân tử đặc biệt và nồng độ cao trong máu đều góp phần vào vai trò của phân tử albumin trong việc điều hòa một loạt các tiến trình sinh lý. Albumin cũng có một số chức năng sinh học, chẳng hạn như liên kết, vận chuyển và khử độc nhiều hợp chất nội sinh và ngoại sinh, tác dụng chống oxy hóa, điều hòa các phản ứng viêm và miễn dịch, ổn định nội mô, điều hòa chức năng đông máu và tiểu cầu. Các đặc tính này được gọi là tác dụng không do tính keo (non-oncotic) vì chúng liên quan trực tiếp đến hình thái và cấu trúc phân tử.
- Nghiên cứu EARSS: albumin 20% 100 mL mỗi 8 giờ trong 3 ngày đầu.
- Nghiên cứu SAFE: hồi sức bằng albumin 4% (bất kỳ khi nào cần bù dịch thay cho dịch tinh thể).
- Nghiên cứu CRISTAL: albumin 4-5% trong nhóm dịch keo với áp suất keo thấp, albumin 20-25% trong nhóm dịch keo với áp suất keo cao.
----
Hồi sức dịch là thực hành tiêu chuẩn cho các tình trạng huyết động không ổn định tương đối hoặc tuyệt đối nhằm phục hồi và duy trì tưới máu mô. Nguy cơ đáng kể của liệu pháp dịch có liên quan đến việc truyền chưa đủ hoặc quá nhiều, cũng như các tác dụng phụ dược lý của loại dịch được sử dụng. Hàng ngày, có hơn 20% bệnh nhân tại các khoa hồi sức tích cực (ICU) được điều trị bằng dịch truyền tĩnh mạch; hơn 30% được truyền dịch để hồi sức thể tích vào ngày thứ nhất nhập ICU.
Ngoại trừ sốc tim, các loại sốc còn lại đều cần hồi sức dịch hoặc cần truyền dịch để làm tăng thể tích tuần hoàn. Những tranh luận về ưu và nhược điểm của từng loại dịch truyền so với loại kia vẫn còn kéo dài và dữ liệu hiện tại chưa thể khẳng định dứt khoát rằng loại dịch nào là tốt nhất. Tùy thuộc vào từng bối cảnh, từng trường hợp và từng thời điểm hồi sức dịch, dịch tinh thể hoặc dịch keo mang lại các lợi ích và tác hại khác nhau. Nếu như dịch tinh thể đã được đồng thuận là loại dịch truyền đầu tay trong hồi sức sốc thì các loại dịch keo, đặc biệt là dung dịch albumin huyết thanh người (human serum albumin - HSA), vẫn có thể có những vai trò nhất định do được giữ lâu trong lòng mạch, có hiệu quả thể tích tốt và ít tác dụng phụ nhưng khá đắt tiền. Việc sử dụng dịch albumin sao cho hiệu quả đòi hỏi hiểu biết tốt về đặc tính sinh lý, chức năng của phân tử albumin, nguyên tắc hồi sức dịch và hiệu quả lâm sàng của dung dịch albumin.
1. Cấu trúc và chức năng của phân tử albumin
Albumin người là một protein đơn phân tan trong nước gồm 585 acid amin với trọng lượng phân tử 66 kDa. Albumin được tổng hợp duy nhất bởi tế bào gan và phóng thích vào tuần hoàn khoảng 13-14 g mỗi ngày trong điều kiện sinh lý (khoảng 0,2 gram albumin trên mỗi kilogram cân nặng). Tuy nhiên, chỉ khoản 40% tổng lượng albumin được giữ trong lòng mạch, phần còn lại được tìm thấy trong dịch kẽ hoặc các cơ quan khác, chẳng hạn như da, cơ và ruột. Nồng độ albumin huyết thanh ở người trưởng thành khỏe mạnh dao động từ 35 đến 50 g/L, chiếm hơn 50% tổng số protein huyết tương và là loại protein lưu hành phong phú nhất trong cơ thể. Sự hiện diện của phân tử albumin trong máu cũng tạo thuận lợi cho sự hấp thu và tái sản xuất albuminliên tục bởi các tế bào gan, dẫn đến tổng thời gian bán hủy của phân tử albumin máu tương đối dài, khoảng 16-20 ngày, nhưng có thể bị rút ngắn do tăng cường dị hóa và thanh thải trong trường hợp có sự thay đổi cấu trúc phân tử albumin, xảy ra trong quá trình lão hóa hoặc tình trạng bệnh lý cấp và mạn tính.Cả cấu trúc phân tử đặc biệt và nồng độ cao trong máu đều góp phần vào vai trò của phân tử albumin trong việc điều hòa một loạt các tiến trình sinh lý. Albumin cũng có một số chức năng sinh học, chẳng hạn như liên kết, vận chuyển và khử độc nhiều hợp chất nội sinh và ngoại sinh, tác dụng chống oxy hóa, điều hòa các phản ứng viêm và miễn dịch, ổn định nội mô, điều hòa chức năng đông máu và tiểu cầu. Các đặc tính này được gọi là tác dụng không do tính keo (non-oncotic) vì chúng liên quan trực tiếp đến hình thái và cấu trúc phân tử.
Albumin liên kết với nhiều loại phân tử, bao gồm bilirubin, acid mật, acid béo, hormone, thuốc và các chất chuyển hóa của thuốc, do đó làm tăng khả năng hòa tan và vận chuyển của chúng đến vị trí tác động hoặc thải trừ. Albumin góp phần vào tính toàn vẹn của mạch máu do liên kết chất nền ngoại bào nội mô giúp điều hòa sự dịch chuyển xuyên mao mạch của dịch. Albumin cũng chống lại rối loạn chức năng nội mô bằng cách làm giảm căng thẳng oxy hóa và nitro hóacũng như sự kết dính tế bào và đáp ứng viêm trong tế bào nội mô.
2. Albumin và áp suất thẩm thấu keo (áp suất keo)
Mặc dù chỉ có khoảng 40% tổng lượng albumin của cơ thể nằm trong lòng mạch nhưng albumin máu chiếm khoảng 70-80% áp suất keo. Do đó, albumin là chất điều biến chính cho sự phân bố dịch giữa các khoang của cơ thể. Đặc tính keo của albumin có từ hiệu quả thẩm thấu liên quan trực tiếp đến khối lượng phân tử của nó (khoảng 2/3) và từ hiệu ứng Gibbs-Donnan (khoảng 1/3), đây là tác dụng liên quan đến việc albumin mang điện tích âm có khả năng thu hút các phân tử tích điện dương, chẳng hạn như natri, làm cho nước dịch chuyển từ ngoại mạch vào nội mạch. Khả năng tạo ra áp suất keo cao hơn của chất keo làm những dung dịch này trở thành lựa chọn hấp dẫn hơn trong hồi sức thể tích vì chúng được cho là duy trì áp suất keo nội mạch cao hơn và do đó giúp làm tăng thể tích nội mạch thay vì rò rỉ ra khoảng kẽ.HSA được dùng trong lâm sàng từ những năm 1940 để duy trì hoặc làm gia tăng thể tích tuần hoàn cũng như điều chỉnh tình trạng giảm albumin máu. Albumin hiện có sẵn dưới dạng dung dịch 4-5% gần như có đồng áp suất keo và đồng áp suất thẩm thấu với huyết thanh người, và dưới dạng dung dịch 20-25% thường được gọi là “albumin đậm đặc”. Khi được truyền vào cơ thể người có trạng thái dịch tốt, albumin 4-5% sẽ làm tăng thể tích huyết tương tương đương với thể tích được truyền; albumin 20-25% sẽ làm tăng thể tích huyết tương khoảng 4-5 lần thể tích truyền. Ở người khỏe mạnh, trên 90% lượng albumin đã truyền được giữ lại trong lòng mạch 2 giờ sau khi truyền, nhưng với các tình huống bệnh nặng, đặc biệt là các trạng thái viêm hệ thống như nhiễm khuẩn huyết nặng thì việc giữ lại albumin đã truyền có thể ít hơn đáng kể.
3. Thoát mao mạch hệ thống
Tình trạng bệnh nặng biểu hiện một trạng thái sinh lý bệnh phức tạp với rối loạn chức năng nhiều cơ quan hệ thống, rối loạn và đáp ứng chuyển hóa được tạo ra để điều chỉnh những rối loạn này. Ở bệnh nhân nặng sau phẫu thuật và bệnh nhân nhiễm khuẩn huyết, có sự thay đổi tính thấm và tăng thoát dịch qua mao mạch làm phá vỡ mối quan hệ này và việc mất dịch vào khoảng kẽ góp phần làm giảm thể tích nội mạch. Hội chứng đáp ứng viêm hệ thống (SIRS) và hội chứng rối loạn chức năng đa cơ quan (MODS) là những dấu hiệu nổi bật của trạng thái sinh lý bệnh như vậy. Trong SIRS có tình trạng giãn mạch và sự rò rỉ mao mạch của dịch được kích hoạt bởi dòng thác đáp ứng viêm phản ứng bởi nhiều tác nhân đáp ứng với tổn thương. Điều này gây ra giảm thể tích tuần hoàn nội mạch do giãn mạch làm tăng lượng máu “tĩnh” trong toàn bộ khoang mạch máu và rò rỉ dịch vào khoảng kẽ do rò rỉ mao mạch. MODS cũng đóng một vai trò quan trọng trong việc quyết định cân bằng dịch của bệnh nhân bị suy tim, tổn thương thận cấp và rối loạn chức năng cơ quan khác tạo ra sự mất cân bằng dịch đáng kể. Rối loạn chuyển hóa kết hợp vấn đề với nhiễm toan, tăng đường huyết và mất cân bằng điện giải liên quan tạo ra một vấn đề có thể làm phức tạp thêm sự cân bằng dịch giữa nội mạch và ngoại mạch.Hiện nay, có nhiều chỉ dấu mới giúp ích cho việc lựa chọn liệu pháp dịch thích hợp bao gồm dấu hiệu rò rỉ mao mạch, nước phổi ngoại mạch và các chỉ số về tính thấm của phổi. Dấu hiệu rò rỉ mao mạch là một tình trạng viêm với nhiều yếu tố kích hoạt khác nhau, xuất phát từ một tiến trình sinh lý bệnh thường gặp bao gồm tái tưới máu sau thiếu máu cục bộ, tạo ra chất chuyển hóa oxy độc hại, tổn thương thành tế bào và enzyme, dẫn đến mất glycocalyx và chức năng hàng rào nội mô mao mạch.
Thoát mao mạch là tình trạng mất dịch, chất điện giải và protein một cách bất thường từ mạch máu vào khoảng kẽ, có khả năng dẫn đến phù nề. Hội chứng tăng tính thấm toàn thể liên quan đến tình trạng viêm hệ thống dai dẳng và liên tục rò rỉ albumin xuyên mao mạch, với cân bằng dịch ròng ngày càng trở nên dương tính. Sau sự tấn công ban đầu của bệnh lý chính rồi đến tổn thương tái tưới máu sau thiếu máu cục bộ, hội chứng tăng tính thấm toàn thể đại diện cho một “cú đánh thứ ba”. Cần tránh tình trạng quá tải dịch trong bối cảnh đặc biệt này.
4. Lớp glycocalyx nội mô
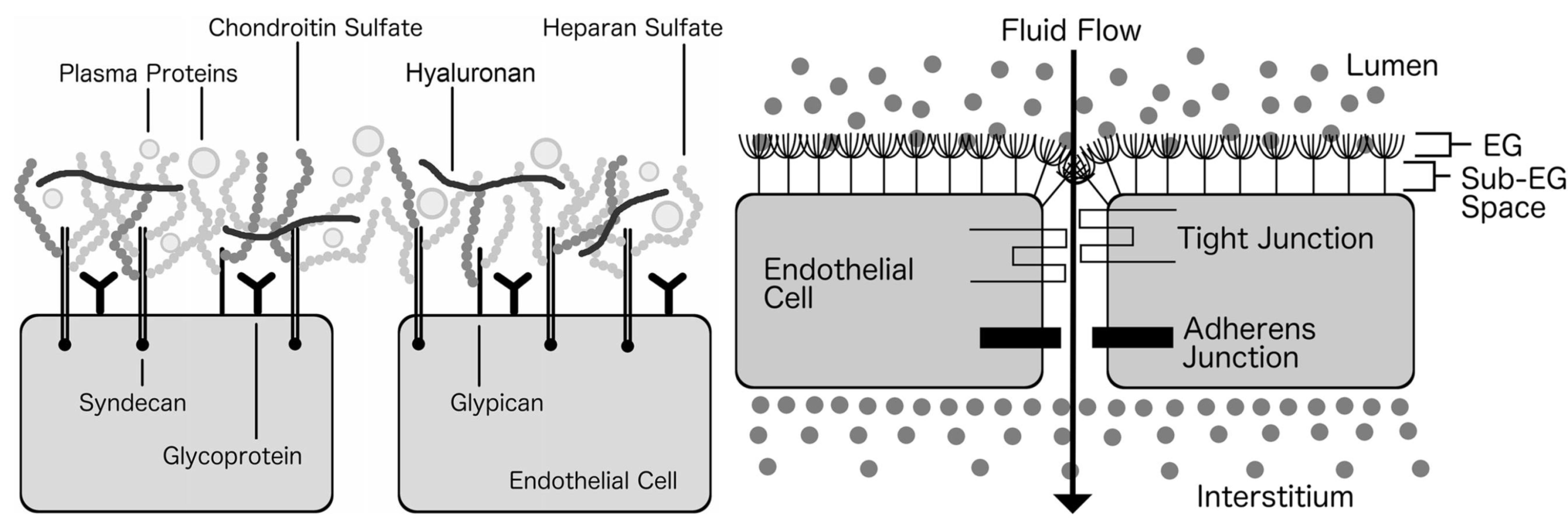
Chức năng nội mô bao gồm đáp ứng viêm và tính thấm được quyết định bởi lớp glycocalyx, là một mạng lưới các proteoglycan và glycoprotein bao phủ bề mặt lòng trong của nội mô mạch máu(Hình 1). Các proteoglycan chính của lớp glycocalyx là các syndecan liên kết xuyên màng và glypican liên kết màng, liên kết với các chuỗi bên glycosaminoglycan, chủ yếu là heparan sulfate nhưng cũng có các loại khác như acid hyaluronic và chondroitin sulfate. Các glycoprotein đa dạng được tìm thấy trong lớp glycocalyx, bao gồm các phân tử kết dính tế bào cũng như các thụ thể liên quan đến tín hiệu gian bào, ly giải fibrin và đông máu. Nhiều phân tử khác có nguồn gốc từ nội mô hoặc huyết tương, bao gồm cả phân tử albumin cũng được tích gộp và mạng lưới khung của lớp glycocalyx. Sự hiểu biết ảnh hưởng của lớp glycocalyx đối với sự chênh lệch áp suất keotrên thành mạch máu đã dẫn đến phương trình Starling “sửa đổi” về sự di chuyển dịch xuyên mạch, mặc dù nguyên tắc này có thể không giải thích đầy đủ cho bản chất động học của hệ tuần hoàn và các quan sát lâm sàng trong các nghiên cứu về liệu pháp dịch.Ở bệnh nhân nặng, glycocalyx nội mô có thể bị tổn thương và việc truyền dung dịch keo có đồng áp suất keo với huyết tương vào những bệnh nhân này sẽ có tác dụng làm tăng thể tích tuần hoàn tương tự như dịch tinh thể. Mức độ tương tự phụ thuộc vào mức độ bong tróc lớp glycocalyx nội mô, tính thấm của glycocalyx nội mô, trạng thái thể tích của bệnh nhân trước khi truyền, tốc độ truyền và mức độ co mạch, và rất khó dự đoán trên lâm sàng do nhiềutương tác phức tạp giữa các biến số liên quan. Điều này có thể giải thích tại sao trong các thử nghiệm lâm sàng lớn trên bệnh nhân nặng, tác dụng làm tăng thể tích tuần hoàn của dịch keo so với dịch tinh thể đã thấp hơn nhiều so với dự đoán.
Hình 1. Lớp glycocalyx nội mô.
5. Albumin bảo tồn lớp glycocalyx
Các thực nghiệm cho thấy việc sửa chữa sớm lớp glycocalyx nội mô có thể cải thiện đáp ứng viêm toàn thân, rối loạn đông máu và khả năng đáp ứng bù dịch sau thiếu máu cục bộ toàn thân hoặc kích thích viêm như nhiễm khuẩn huyết nặng hoặc chấn thương lớn. Khung thời gian để lớp glycocalyx nội mô tự phục hồi về mặt lâm sàng mà không có bất kỳ sự can thiệp nào khoảng 5-7 ngày sau khi ngừng các kích thích gây bong tróc trong nghiên cứu trên mô hình chuột và thí nghiệm nuôi cấy tế bào nội mô ở người. Do đó, có một cửa sổ trong khung thời gian tương đối dài để can thiệp nhằm kích thích sửa chữa sớm hơn. Ngày càng có nhiều bằng chứng cho thấy các loại dịch hồi sức thường được sử dụng có các khả năng khác nhau trong việc bảo vệ và phục hồi lớp glycocalyx nội mô.Môi trường có hàm lượng protein thấp là nguyên nhân gây ra sự phá hủy hoặc bong tróc nhanh chóng của glycocalyx nội mô. Hiện tượng này không phụ thuộc vào ảnh hưởng của áp suất thẩm thấu, vì đối với cùng một áp suất thẩm thấu nội mạch, huyết tương và albumin có hiệu quả hơn các chất keo bán tổng hợp như tinh bột hydroxyetyl (HES) trong việc bảo tồn và phục hồi glycocalyx nội mô, làm giảm tính thấm thành mạch và giảm sự kết tập tiểu cầu và bạch cầu. Cơ chế của “tác dụng chữa lành” vượt trội của albumin và huyết tương vẫn chưa hoàn toàn rõ ràng và được gọi là “nghịch lý áp suất thẩm thấu keo”.
Ban đầu, người ta cho rằng việc tưới vào nội mạc bằng dung dịch không có protein sẽ làm hư hại lớpglycocalyx nội mô do rửa trôi các protein tích hợp của lớp này. Tuy nhiên, phương pháp nhuộm hóa mô miễn dịch và kính hiển vi điện tử đã phát hiện rằng môi trường ít protein gây ra sự thiếu vắng hoàn toàn, chứ không phải là hư hại, của glycocalyx nội mô. Điều này dường như là do sự phân cắt ma trận metalloproteinase (MMP) của các thành phần glycocalyx khỏi lớp nội mô bên dưới. Tác dụng bảo vệ của protein có thể được trung gian bởi một chất liên kết với protein ức chế sự phân cắt MMP của glycocalyx nội mô, chẳng hạn như chất trung gian lipid sphingosine 1-phosphate (S1P). Hồng cầu và tiểu cầu là nguồn chính của S1P trong cơ thể, trong khi đó protein huyết tương, chủ yếu là lipoprotein mật độ cao (HDL) và albumin, tạo điều kiện thuận lợi cho việc giải phóng S1P từ các nguồn này. Có thể là albumin giúpphục hồi glycocalyx nội mô, nhưng sự phục hồi này không thay đổi kết cục lâm sàng. Cũng có thể là do nồng độ albumin lưu hành cần phải giảm xuống dưới mức quan trọng trước khi bổ sung để có bất kỳ tác dụng đáng kể nào về mặt lâm sàng. Hoặc, có thể bản thân albumin không phải là chất trung gian của quá trình sửa chữa glycocalyx nội mô, mà là một chất trung gian khác có trong dung dịch albumin, chẳng hạn như S1P.
6. Hạ albumin máu
Hạ albumin máu rất thường gặp ở bệnh nhân nằm viện và bệnh nặng. Các cơ chế có thể góp phần vào tình trạng này có thể là giảm sản xuất (nguyên nhân không phổ biến do rối loạn chức năng gan), tăng mất albumin vào khoang thứ ba (trong nhiễm khuẩn huyết và bỏng) hoặc pha loãng máu do sử dụng một lượng lớn dịch tinh thể, hoặc mất qua thận (bệnh thận mạn và hội chứng thận hư), mất đường tiêu hóa (bệnh crohn hoặc tăng áp mạch bạch huyết), mất máu, hoặc do tăng dị hóa albumin. Hạ albumin máu có liên quan đến tăng bệnh suất và tử suất, kéo dài thời gian nằm hồi sức và thời gian nằm viện cũng như tăng chi phí điều trị. Mối liên quan giữa giảm albumin máu và kết cục kém dường như không phụ thuộc vào tình trạng dinh dưỡng và tình trạng viêm; tỷ lệ biến chứng có thể giảm khi nồng độ albumin máu đạt được trên 30 g/L.7. HIỆU QUẢ LÂM SÀNG CỦA DUNG DỊCH ALBUMIN
Tranh luận về dịch keo và dịch tinh thể trong hồi sức bệnh nhân nặng đã kéo dài vài thập kỷ. Vấn đề dường như bắt nguồn từ tính an toàn, hiệu quả và tỷ lệ lợi ích/nguy cơ của việc sử dụng dịch keo so với dịch tinh thể và chi phí cao của HSA so với chi phí tương đối thấp của dịch tinh thể. Một câu hỏi cụ thể quan trọng là việc sử dụng hoặc công dụng của albumin trong quá trình hồi sức bệnh nhân nhiễm khuẩn nặng/bệnh nhân nặng.Hầu hết các khuyến cáo đều thừa nhận vai trò của HSA trong hồi sức thể tích bệnh nhân nặng, đặc biệt là trong sốc nhiễm khuẩn. Thông thường, HSA được chỉ định khi cần truyền một lượng dịch lớn trong giai đoạn hồi sức cứu mạng (resuscitation) và tối ưu hóa (optimization) nhằm tiết chế truyền dịch quá nhiều sẽ dẫn đến phù nề và quá tải dịch sau đó, cả hai biến chứng này đều dẫn đến kết cục xấu. HSA cũng góp phần vào cân bằng dịch âm trong giai đoạn ổn định (stabilization) và xuống thang (evacuation). Mặc dù không có nhiều thử nghiệm lâm sàng khẳng định dứt khoát vai trò của dung dịch albumin trong các bối cảnh lâm sàng khác nhau, nhưng nhìn chung albumin là một dung dịch an toàn cho chỉ định bù dịch và không có tác hại nào liên quan đến việc sử dụng HSA.
7.1 HSA ở bệnh nhân hồi sức chung
Một thử nghiệm lâm sàng ngẫu nhiên với gần 7000 bệnh nhân nhằm so sánh tỷ lệ tử vong và tính an toàn khi sử dụng muối đẳng trương hoặc albumin 4% trong một quần thể bệnh nhân ICU hỗn hợp (nghiên cứu SAFE). Cho đến nay, nghiên cứu mang tính bước ngoặt này vẫn được xem là bằng chứng quan trọng khi đánh giá lợi ích của việc hồi sức bằng albumin ở bệnh nhân nặng. Mặc dù kết cục chính (tử vong 28 ngày, ngày nằm hồi sức, ngày nằm viện, ngày thở máy và ngày điều trị thay thế thận) là tương tự ở hai nhóm nhưng phân tích dưới nhóm cho thấy nhánh albumin có xu hướng giảm tỷ lệ tử vong ở bệnh nhân sốc nhiễm khuẩn và xu hướng tăng tỷ lệ tử vong ở bệnh nhân chấn thương, đặc biệt chấn thương sọ não. Đồng thời, albumin 4% cũng không có lợi ích về tử vong ở bệnh nhân bỏng. Tuy nhiên, dường như HSA vẫn có lợi cho một vài nhóm bệnh nhân chọn lọc nào đó. Sau đó, nghiên cứu CRISTAL trên 2800 bệnh nhân ICU hỗn hợp, đã cho thấy nhánh sử dụng dịch keo (gelatin, dextran, HES, albumin 4% và 20%) giảm tỷ lệ tử vong 28 ngày và 90 ngày so với dịch tinh thể. Việc sử dụng albumin có liên quan đến nồng độ chloride cao hơn trong quá trình hồi sức thể tích lớn. Sự khác biệt thực tế có vẻ nhỏ so với thể tích dịch, mức độ bệnh nặng và thời gian mắc bệnh dường như là lý do quan trọng hơn dẫn đến những kết cục này. Một phân tích hậu định của nghiên cứu SAFE cho thấy thời gian đông máu kéo dài khi hồi sức bằng albumin 4% và thể tích lớn hơn được truyền.Quảng cáo
Cả albumin 4% và 20% đều được chứng minh là an toàn và có liên quan đến tăng thể tích nhát bóp cùng với giảm hậu tải so với dịch tinh thể. Trước đây HSA được sử dụng kết hợp với thuốc lợi tiểu và sự kết hợp này dường như cải thiện oxy hóa, ổn định huyết động và đạt được cân bằng dịch âm tốt hơn ở bệnh nhân tổn thương phổi cấp. Mặc dù giảm albumin máu làm tăng tỷ lệ tử vong, nhưng phân tích hậu định từ nghiên cứu SAFE cho thấy việc sử dụng albumin để hồi sức thể tích cho bệnh nhân nặng với nồng độ albumin huyết thanh ≤25 g/L không liên quan đến cải thiện tử vong, thời gian nằm hồi sức hoặc thở máy, hoặc điều trị thay thế thận (các kết cục này tương tự nhóm albumin huyết thanh >25 g/L). Những thực hành như vậy, chẳng hạn như sử dụng albumin “thường quy” để làm tăng nồng độ albumin huyết thanh ở bệnh nhân hồi sức ngoại khoa, là không có bằng chứng và có thể không mang lại bất kỳ lợi ích lâm sàng nào.
7.2 HSA trong hồi sức nhiễm khuẩn huyết và sốc nhiễm khuẩn
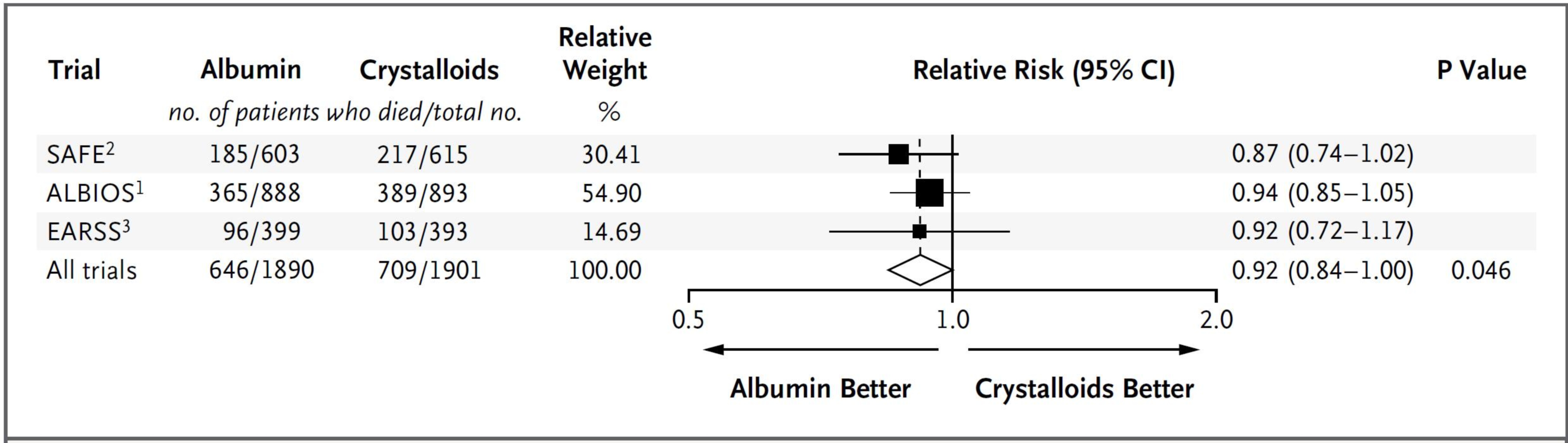
Liệu pháp HSA cho bệnh nhân nhiễm khuẩn huyết được đánh giá trong ba thử nghiệm lâm sàng quy mô lớn, hai nghiên cứu ALBIOS và EARSS đều sử dụng albumin 20% có liên quan đến những bệnh nhân bị hạ albumin máu ở thời điểm nhận vào nghiên cứu, và một phân tích phụ được chỉ định trước từ nghiên cứu SAFE. Ảnh hưởng của HSA lên tỷ lệ tử vong không đạt ý nghĩa thống kê trong các phân tích chính của các thử nghiệm riêng lẻ. Với nghiên cứu ALBIOS, một phân tích hậu định về phân nhóm bệnh nhân sốc nhiễm khuẩn cho thấy tỷ lệ tử vong 90 ngày giảm đáng kể ở nhánh albumin 20% so với nhánh dịch tinh thể. Với nghiên cứu SAFE, phân tích đa biến hiệu chỉnh cho các đặc điểm nền (ở những bệnh nhân có dữ liệu đầy đủ, n = 919) cho thấy HSA có liên quan đến giảm odds tử vong so với muối đẳng trương. Mặc dù có sự khác biệt về thiết kế và tiêu chí cho ba nghiên cứu này nhưng một phân tích tổng hợp gợi ý rằng nguy cơ tử vong gộp thấp hơn đáng kể trong ba thử nghiệm (RR 0,92, KTC 95%: 0,84-1,00; p = 0,046) ở bệnh nhân nhiễm khuẩn huyết nặng được điều trị bằng HAS (Biểu đồ).Biểu đồ 1. Ưu thế của dung dịch albumin trong sốc nhiễm khuẩn.
7.3 Albumin bảo vệ thận
Chức năng sinh lý của albumin bao gồm cả việc vận chuyển các chất không tan trong nước, đệm acid-base, chống viêm và chống oxy hóa, tất cả đều có khả năng góp phần vào ảnh hưởng thuận lợi của albumin đối với chức năng tế bào và cơ quan ở bệnh nhân nặng ngoài hiệu quả huyết động do bảo toàn áp suất keo. Hơn nữa, albumin nội sinh có liên quan, thông qua các con đường dẫn truyền tín hiệu khác nhau, duy trì tính toàn vẹn và chức năng của tế bào ống lượn gần thông qua tác động điều hòa tăng sinh.7.4 Cân bằng dịch âm và loại bỏ dịch hồi sức
Việc truyền dịch lượng lớn trong giai đoạn hồi sức dịch góp phần vào tình trạng thừa dịch ở bệnh nhân nặng. Phù nề thường trở nên nghiêm trọng hơn do giảm albumin máu và có thể là nguyên nhân dẫn đến việc cai máy thở khó khăn và liên quan đến biến chứng ở các cơ quan khác nhau và tăng tỷ lệ tử vong. Ngay cả khi quá tải dịch từ 5% đến 10% trọng lượng cơ thể ở bệnh nhân nặng cũng có liên quan đến thở máy kéo dài, giảm trao đổi khí, chậm lành vết thương sau phẫu thuật và rối loạn đông máu. Thông thường, việc dùng thuốc lợi tiểu để khôi phục cân bằng dịch tối ưu được xem là điều trị tiêu chuẩn.Phù thường gặp ở những bệnh nhân hội chứng thận hư được cho là có liên quan đến giảm albumin máu do mất albumin tại thận, và HSA đã được sử dụng để điều trị phù kháng thuốc lợi tiểu ở bệnh nhân này. Việc sử dụng HSA có thể làm tăng tác dụng của furosemide ở bệnh nhân hội chứng thận hư, điều này liên quan những thay đổi huyết động tại thận do truyền albumin đã được chứng minh ở bệnh nhân xơ gan và AKI mất bù cấp tính. Nồng độ albumin thấp nghiêm trọng cản trở sự bài tiết furosemide trong lòng ống thận dẫn đến tình trạng kháng thuốc lợi tiểu. Mức độ kháng furosemide có thể phụ thuộc vào mức độ nặng của tình trạng giảm albumin máu. Dùng furosemide đơn độc làm tăng đáng kể lượng natri bài tiết trong nước tiểu và lượng nước tiểu so với chỉ dùng albumin đơn độc. Việc sử dụng đồng thời furosemide và HSA làm tăng tác dụng của furosemide và nồng độ của yếu tố lợi tiểu natri tâm nhĩ, cũng như tăng nồng độ albumin huyết thanh.
Sự tích tụ dịch trong phổi của bệnh nhân bị tổn thương phổi cấp có xu hướng tăng lên khi nồng độ protein huyết thanh thấp. Những bệnh nhân này có thể đáp ứng tốt hơn với sự kết hợp của thuốc lợi tiểu và albumin, hơn là chỉ dùng furosemide. Trong một nghiên cứu đối chứng trên bệnh nhân ARDS có nồng độ protein huyết thanh dưới 60 g/L thì những người được truyền albumin cộng với furosemide có khả năng oxy hóa tốt hơn và nồng độ protein trong huyết thanh tốt hơn so với nhóm chỉ được truyền furosemide và tình trạng giữ nước ít hơn đáng kể (cân bằng dịch ròng âm tính hơn); nhóm chứng thì bị tình trạng hạ huyết áp thường xuyên hơn và số ngày dùng thuốc vận mạch nhiều hơn. Do đó, trong tình huống lâm sàng này, cân bằng dịch âm nhằm mục đích bảo vệ có thể dễ dàng đạt được hơn khi truyền HSA.
Áp lực tĩnh mạch trung tâm cao liên quan đến tổn thương thận cấp (AKI) ở bệnh nhân hồi sức ngoại khoa bị nhiễm khuẩn huyết nặng. Sự gia tăng áp lực tĩnh mạch thận có thể trực tiếp gây ra tình trạng giữ natri tại thận và có thể làm tăng áp lực tĩnh mạch thận thêm nữa. Cân bằng dịch dương tích lũy sau khi truyền lượng dịch hồi sức ban đầu trong sốc nhiễm khuẩn có thể là một kịch bản hồi sức đang ngày càng được chú ý. Ở những bệnh nhân này, chức năng bài tiết dịch qua thận đã bị suy giảm dẫn đến phù nề mô kẽ góp phần làm chậm phục hồi chức năng thận. Do đó, các chiến lược truyền dịch thận trọng ngày càng được ủng hộ. Mục tiêu bù dịch cần phải được xác định cẩn thận và đánh giá chính xác tình trạng dịch, không chỉ trong giai đoạn sớm ARDS mà còn trong hồi sức dịch ở bệnh nhân nhiễm khuẩn huyết nặng và sốc nhiễm khuẩn.
7.5 Albumin 5% hay 20%?
Gần đây dung dịch muối có tính đệm và albumin 20% đã được ủng hộ như một loại dịch được dùng hồi sức thể tích nhỏ. Dịch keo làm căng tâm nhĩ trái nhiều hơn, giảm thể tích phổi và tăng khả năng khuếch tán hơn so với dịch tinh thể, nhưng không gây phù phổi. Dịch keo cũng làm tăng thể tích nhát bóp nhiều hơn và có liên quan đến giảm hậu tải. Hiệu suất của tim được tăng lên nhờ thể tích dịch truyền albumin 20% nhỏ hơn khi so sánh với albumin 4%. Albumin 20% gây ra sự thay đổi tối thiểu nồng độ các chất điện giải trong huyết thanh ngoại trừ sự giảm nồng độ calci. Nghiên cứu ngẫu nhiên SWIPE trên 321 bệnh nhân hồi sức hỗn hợp nhằm so sánh nhu cầu thể tích hồi sức, cân bằng dịch, hiệu quả sinh hóa và sinh lý của albumin 20% so với albumin 4–5%. Kết quả cho thấy thể tích dịch hồi sức tích lũy sau 48 giờ thấp hơn, nồng độ albumin máu tối đa cao hơn nhưng nồng độ natri và chloride thấp hơn ở nhóm albumin 20%.8. Kết luận
Dù có giá thành cao hơn và bằng chứng hạn chế để sử dụng cho bệnh nhân nặng nhưng albumin vẫn tiếp tục là dung dịch keo được lựa chọn rộng rải trên toàn thế giới. Mặc dù đã được chứng minh giúp làm giảm cân bằng dịch tổng thể cũng như góp phần làm tăng thể tích nội mạch nhưng các nghiên cứu lặp lại đã không chứng minh được hiệu quả như vậy và không cải thiện kết cục sống còn. Trong bối cảnh thiếu lựa chọn loại dung dịch keo khác do các tác dụng phụ, albumin vẫn được chấp nhận là một trong những loại dịch hồi sức quan trọng hiện nay và trong tương lai gần.ĐỌC THÊM
1. Bhavani S.S., Khanna A.K., Mathur P. (2020) Albumin in the Critically Ill. In: Perioperative Fluid Management. Springer, Cham. https://doi.org/10.1007/978-3-030-48374-6_11Quảng cáo
2. Farag E., Ebrahim Z.Y. (2016) The Perioperative Use of Albumin. In: Perioperative Fluid Management. Springer, Cham. https://doi.org/10.1007/978-3-319-39141-0_9
3. Finfer S. Reappraising the role of albumin for resuscitation. Curr Opin Crit Care. 2013 Aug;19(4):315-20. doi: 10.1097/MCC.0b013e3283632e42
4. Milford, E.M., Reade, M.C. Resuscitation Fluid Choices to Preserve the Endothelial Glycocalyx. Crit Care 23, 77 (2019). https://doi.org/10.1186/s13054-019-2369-x
5. Jean Louis Vincent, Daniel De Backer, Christian J. Wiedermann. Fluid management in sepsis: The potential beneficial effects of albumin. Journal of Critical Care, Volume 35 (2016). https://doi.org/10.1016/j.jcrc.2016.04.019
6. Caironi P, Tognoni G, Masson S, Fumagalli R, et al; ALBIOS Study Investigators. Albumin replacement in patients with severe sepsis or septic shock. N Engl J Med. 2014 Apr 10;370(15):1412-21. doi: 10.1056/NEJMoa1305727
7. Finfer S, Bellomo R, Boyce N, French J, Myburgh J, Norton R; SAFE Study Investigators. A comparison of albumin and saline for fluid resuscitation in the intensive care unit. N Engl J Med. 2004 May 27;350(22):2247-56. doi: 10.1056/NEJMoa040232
8. Annane D, Siami S, Jaber S, Martin C, et al; CRISTAL Investigators. Effects of fluid resuscitation with colloids vs crystalloids on mortality in critically ill patients presenting with hypovolemic shock: the CRISTAL randomized trial. JAMA. 2013 Nov 6;310(17):1809-17. doi: 10.1001/jama.2013.280502
9. Vincent JL, Dubois MJ, Navickis RJ, et al. Hypoalbuminemia in acute illness: is there a rationale for intervention? A meta-analysis of cohort studies and controlled trials. Ann Surg. 2003 Mar;237(3):319-34.
10. Martin GS, Bassett P. Crystalloids vs. colloids for fluid resuscitation in the Intensive Care Unit: A systematic review and meta-analysis. J Crit Care. 2019 Apr;50:144-154.
11. Mårtensson J, Bihari S, Bannard-Smith J, et al. Small volume resuscitation with 20% albumin in intensive care: physiological effects : The SWIPE randomised clinical trial. Intensive Care Med. 2018 Nov;44(11):1797-1806. doi: 10.1007/s00134-018-5253-2
12. Wiedermann CJ, Joannidis M. Albumin replacement in severe sepsis or septic shock. N Engl J Med. 2014 Jul 3;371(1):83.